こんにちは。行政書士の孔です。
医療機器を日本で取り扱いたいと考えたとき、多くの事業者が最初に迷うのが「この製品はクラスIなのか、クラスIIなのか」「認証で足りるのか、それとも承認が必要なのか」という点です。
特に海外メーカー様や新規参入される方の場合、海外では同じようなカテゴリーで販売されていても、日本では一般的名称(JMDN)や使用目的、構造、既存基準との関係によって手続の重さが変わるため、感覚だけで進めるとかなり危険です。PMDAも、医療機器の製造販売にあたっては、生体へのリスクの大きさに応じて、届出、第三者認証、大臣承認と手続が分かれると説明しています。
そのため、実務では「まず認証が取れそうか」を考えるより先に、
どの一般的名称に当たるのか、
その一般的名称のクラスは何か、
認証基準があるのか、
認証基準がないなら承認案件なのか、
を順に整理していく方が安全です。
医療機器のクラスは「リスクの大きさ」で決まる
日本の医療機器は、国際的なリスク分類の考え方を踏まえて、クラスI、クラスII、クラスIII、クラスIVに分けられています。PMDAと厚生労働省の資料では、クラスIは一般医療機器、クラスIIは管理医療機器、クラスIII・IVは高度管理医療機器として整理され、リスクが上がるにつれて手続も重くなると説明されています。
ここで大切なのは、「クラスが高いほど難しい」という単純な理解で終わらないことです。
実際には、クラスIIだから必ず認証、クラスIIIだから必ず承認、というわけではなく、認証基準があるかどうかで分岐する場面があります。特にクラスIIは認証基準があるものが多く、クラスIIIでも一部は第三者認証の対象になっています。
医療機器のクラス別早見表
| クラス | 区分 | 主な手続の考え方 | 代表例 | 実務上の見方 |
|---|---|---|---|---|
| クラスI | 一般医療機器 | 原則として届出 | 鋼製小物、X線フィルム、歯科技工用用品 など | まずは一般的名称(JMDN)を確認し、届出で足りるかを見る |
| クラスII | 管理医療機器 | 認証基準があれば第三者認証、なければ承認の可能性 | 電子式血圧計、超音波診断装置、電子内視鏡、消化器用カテーテル など | 「クラスIIだから認証」と決めつけず、認証基準の有無を確認する |
| クラスIII | 高度管理医療機器 | 承認が基本。ただし認証基準がある一部は第三者認証 | 人工呼吸器、人工骨・関節、透析器、バルーンカテーテル など | 高度管理でも一律ではなく、認証基準の有無で分かれる |
| クラスIV | 高度管理医療機器 | 原則として承認 | ペースメーカー、人工心臓弁、ステント など | 生命への影響が大きく、最初から承認案件として考えることが多い |
クラスIは「一般医療機器」
クラスIは、不具合が生じた場合でも人体へのリスクが極めて低いと考えられる機器です。
PMDAの説明では、クラスIはPMDAへの届出によって製造販売が可能な一般医療機器として位置付けられています。厚生労働省の資料でも、クラスIは承認・認証不要で、届出/自己認証の区分と整理されています。
代表例としては、厚生労働省資料に、体外診断用機器、鋼製小物、X線フィルム、歯科技工用用品が挙げられています。
「鋼製小物」というと少し分かりにくいですが、実務上イメージしやすいのは、メス、ピンセット、鉗子のような比較的シンプルな器具です。こうしたものは、医療機器ではあっても、一般にリスクは低いと整理されやすく、まずは届出の枠組みから考えることになります。
ただし、同じように見える器具でも、構造や使用目的、滅菌の有無、侵襲性などによって一般的名称やクラスが変わる可能性があります。
そのため、「見た目がシンプルだからクラスIだろう」と判断するのではなく、JMDNの一般的名称ベースで確認することが必要です。
クラスIIは「管理医療機器」
クラスIIは、不具合が生じた場合でも人体へのリスクが比較的低いと考えられる管理医療機器です。
PMDAは、クラスIIのうち認証基準のあるものについては、登録認証機関による第三者認証が必要だと説明しています。一方、厚生労働省資料では、認証基準がない、または認証基準に適合しないクラスIIは、大臣承認の対象になると整理されています。
代表例としては、MRI、電子式血圧計、電子内視鏡、消化器用カテーテル、超音波診断装置、歯科用合金が挙げられています。
事業者の感覚としては、電子血圧計や超音波診断装置のように、すでに市場に一定の標準があり、既存技術として整理しやすい機器は、認証基準に乗る可能性をまず検討することになります。
ただし、ここで注意したいのは、クラスIIだから安心して認証で行けるとは限らないという点です。
たとえば、新しい構造や追加機能がある、既存認証基準にうまく当てはまらない、一般的名称の選び方が微妙、といった場合には、認証ではなく承認側で見る必要が出ることがあります。実務では、ここを見誤ると、最初のスケジュール感が大きくずれます。
クラスIIIは「高度管理医療機器」
クラスIIIは、不具合が生じた場合に人体へのリスクが比較的高いと考えられる高度管理医療機器です。
PMDAは、クラスIII・IVは大臣承認が必要でPMDAが審査を行うと説明する一方で、2014年11月25日以降、クラスIIIのうち認証基準のあるものは第三者認証が可能と明記しています。つまり、クラスIIIは「承認が基本、ただし一部認証あり」と理解するのが実務に近いです。 (pmda.go.jp)
厚生労働省資料にある代表例は、透析器、人工骨・関節、人工呼吸器、バルーンカテーテルです。
このあたりになると、生体への影響が比較的大きく、品質・安全性・性能に対する要求も高くなるため、一般に審査の重みも増します。特に人工骨や人工関節のような埋植系、人工呼吸器のような生命維持に関わる機器は、事業者としても「認証で簡単に行ける」という発想は持たない方がよい領域です。 (厚生労働省)
一方で、クラスIIIでも認証基準がある場合には、第三者認証の可能性が残ります。
したがって、クラスIII案件では「高度管理だから即PMDA承認」と決め打ちせず、認証基準の有無を必ず確認することが重要です。 (pmda.go.jp)
クラスIVも「高度管理医療機器」である
クラスIVは、患者への侵襲性が高く、不具合が生じた場合に生命の危険に直結するおそれのある高度管理医療機器です。
厚生労働省資料では、代表例としてペースメーカー、人工心臓弁、ステントが挙げられています。PMDAの整理でも、クラスIVは承認対象としてPMDA審査に乗る区分です。 (厚生労働省)
このあたりは、事業者としても「認証か承認か」で迷うというより、最初から承認案件として体制・資料・スケジュールを組むことが多い領域です。
特に植込み型や心血管系などの機器では、臨床評価、品質管理、リスクマネジメント、海外データの扱いなど、検討事項が重くなりやすいため、初期段階での分類確認がより重要になります。 (pmda.go.jp)
「認証」とは何か?
なぜクラスIIや一部クラスIIIで問題になるのか
医療機器の「認証」とは、登録認証機関が、対象機器が定められた認証基準に適合しているかを確認し、製造販売を認める仕組みです。
厚生労働省の資料では、クラスIIの管理医療機器のうち認証基準に適合するもの、そしてクラスIIIのうち認証基準のあるものが、この第三者認証の対象になります。
事業者目線でいうと、「認証」で進められる案件は、ある程度、既存の標準や評価軸に乗せやすい案件です。
逆に、認証基準に合わない、認証基準が存在しない、あるいはその医療機器が従来品とかなり違う場合には、承認申請に回る可能性があります。つまり、「クラス」だけでなく、認証基準との距離感が実務ではとても大切です。
事業者が最初にやるべきこと
クラス名を覚えるより、「一般的名称」と「認証基準」を見ることです
新規参入者や海外メーカーがやりがちなのは、「うちの製品はたぶんクラスIIくらいだろう」「似た製品が認証だからうちも認証だろう」と先に決めてしまうことです。
けれども、実務では、まず一般的名称(JMDN)を確認し、その名称に紐づくクラス分類を確認し、その上で認証基準の有無を見る流れが基本です。PMDAの一般的名称検索システムも、まさにそのために使われています。
つまり、事業者が最初に見るべき順番は、次のようになります。
「この製品は日本でどの一般的名称に当たるのか」
「その一般的名称はクラスI・II・III・IVのどれか」
「認証基準はあるのか」
「認証基準に素直に乗るのか、それとも承認案件か」
この順序で考えると、届出、認証、承認の見通しがかなり立てやすくなります。
よくある誤解
クラスIIなら全部認証で進められる
そうとは限りません。クラスIIでも、認証基準がない、または基準に適合しない場合は承認申請側になることがあります。
クラスIIIなら全部承認になる
承認が基本ですが、認証基準があるクラスIIIは第三者認証が可能です。
見た目が簡単そうな機器ならクラスIだろう
見た目では決まりません。一般的名称、使用目的、構造、侵襲性などを踏まえて判断する必要があります。
海外での分類と同じ感覚で日本でも進められる
必ずしも同じではありません。日本ではJMDN一般的名称と国内基準の有無が重要になります。
まとめ
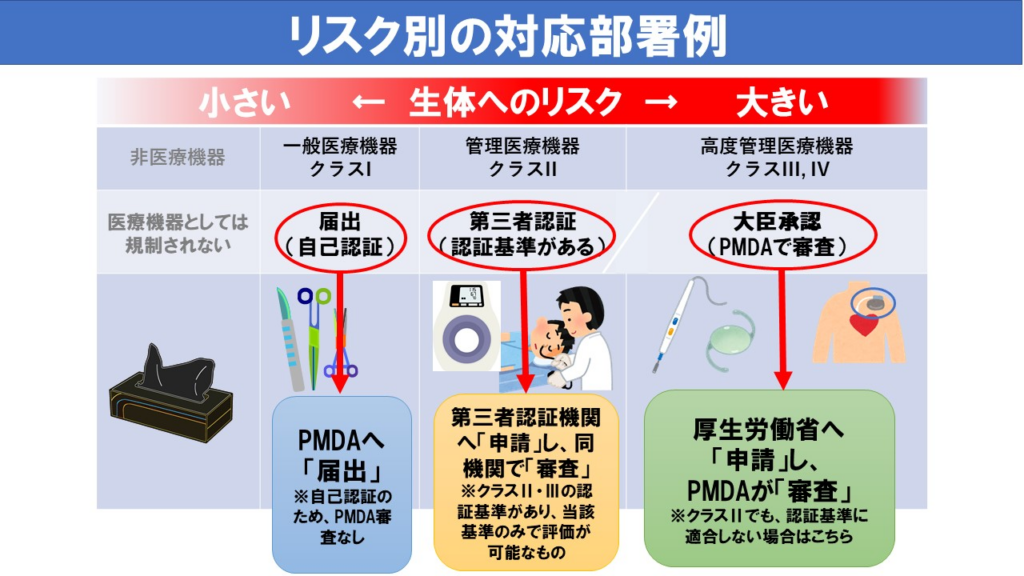
医療機器のクラスは、単に難易度を4段階で並べたものではなく、生体リスクに応じて、届出・認証・承認のどのルートで進むかを決める出発点です。
クラスIは届出、クラスIIは認証基準があれば第三者認証、クラスIII・IVは承認が基本で、クラスIIIの一部は認証もあり得る、というのが基本構造です。
ただし、実務で本当に大切なのは、クラス名を暗記することではありません。
自社製品の一般的名称は何か、認証基準はあるのか、その基準に素直に乗るのかを見ていくことです。
MRI、電子式血圧計、超音波診断装置、人工呼吸器、人工関節、ペースメーカーといった具体例を頭に入れておくと、クラス感覚はつかみやすくなりますが、最終的には個別製品ごとの確認が必要です。